ৰাসায়নিক বিক্ৰিয়া আৰু সমীকৰণ - সাৰাংশ
SEBA দশম শ্ৰেণীৰ বিজ্ঞানৰ 'ৰাসায়নিক বিক্ৰিয়া আৰু সমীকৰণ' অধ্যায়ৰ পৃষ্ঠা ৬ ত থকা প্ৰশ্নাৱলীৰ অসমীয়া মাধ্যমৰ সমাধান। এই সমাধানত সংযোজন, বিযোজন, অপসৰণ, আৰু দ্বিঅপসৰণ বিক্ৰিয়াৰ উদাহৰণসহ সন্তুলিত ৰাসায়নিক সমীকৰণসমূহ অন্তৰ্ভুক্ত। বিস্তারিত সমাধানৰ বাবে, অনুগ্ৰহ কৰি তলৰ লিংকত ক্লিক কৰক।
Follow Us
| Join Now | |
| Join Now | |
| Telegram | Join Now |

অসম মাধ্যমিক শিক্ষা পৰিষদ (SEBA) অসমৰ দশম শ্ৰেণীৰ শিক্ষাৰ বাবে পাঠ্যক্ৰম নিৰ্ধাৰণ, পৰীক্ষা পৰিচালনা আৰু প্ৰমাণপত্ৰ প্ৰদান কৰে। এই পৰ্যায়ত শিক্ষাৰ্থীসকলে বিভিন্ন বিষয় অধ্যয়ন কৰে, যেনেঃ অসমীয়া, ইংৰাজী, গণিত, বিজ্ঞান, সমাজ বিজ্ঞান, আৰু বাণিজ্যিক শিক্ষা।
পাঠ্যক্ৰম আৰু পাঠ্যপুথি
SEBA-ৰ দ্বাৰা প্ৰদান কৰা পাঠ্যক্ৰমৰ অধীনত দশম শ্ৰেণীৰ শিক্ষাৰ্থীসকলে নিম্নলিখিত বিষয়সমূহ অধ্যয়ন কৰে
- অসমীয়া : এই বিষয়ত অসমীয়া সাহিত্য, ব্যাকৰণ আৰু ৰচনা অন্তৰ্ভুক্ত থাকে।
- ইংৰাজী : ইংৰাজী ভাষাৰ সাহিত্য আৰু ব্যাকৰণৰ অধ্যয়ন কৰা হয়।
- গণিত : বাস্তৱ সংখ্যা, বহুপদ, ত্ৰিকোণমিতি, স্থানাংক জ্যামিতি, বৃত্ত, পৰিসংখ্যা আদি অধ্যায় অন্তৰ্ভুক্ত।
- বিজ্ঞান : ৰসায়ন, জীৱবিজ্ঞান, পদাৰ্থ বিজ্ঞান আৰু পৰিৱেশ বিজ্ঞানৰ বিভিন্ন অধ্যায় অন্তৰ্ভুক্ত।
- সমাজ বিজ্ঞান : ইতিহাস, ভূগোল, ৰাজনীতি বিজ্ঞান আৰু অৰ্থনীতিৰ অধ্যয়ন কৰা হয়।
- উচ্চ গণিত : সিদ্বান্ত, সমীকৰণ, পৰিসংখ্যা, কেলকুলাছ, আৰু আন বহু কিছু। শিক্ষাৰ্থীসকলৰ বাবে প্রস্তুতি আৰু পাঠ্যসূচীসহ পাঠ্যবইৰ সহজ ব্যাখ্যা।
প্ৰতিটো বিষয়ৰ বাবে SEBA-ৰ দ্বাৰা নিৰ্ধাৰিত পাঠ্যপুথি ব্যৱহাৰ কৰা হয়। এই পাঠ্যপুথিসমূহ SEBA-ৰ চৰকাৰী ৱেবছাইটত উপলব্ধ।

♦ তোমালোকে কি শিকিলা
- এটা সম্পূৰ্ণ ৰাসায়নিক সমীকৰণে বিক্রিয়া, বিক্রিয়াজাত পদার্থ আৰু সিহঁতৰ ভৌতিক অৱস্থাক সাংকেতিক ৰূপত উপস্থাপন কৰে।
- ৰাসায়নিক বিক্রিয়া এটাক সন্তুলিত কৰা হয় যাতে সমীকৰণটোৰ বিক্রিয়ক আৰু বিক্রিয়াজাত পদাৰ্থৰ প্রতিবিধ পৰমাণুৰ সংখ্যা একে হয়। সমীকৰণসমূহ সদায় সন্তুলিত হ'ব লাগিব।
- এটা সংযোজন বিক্রিয়াত দুটা বা ততোধিক পদার্থ লগ হৈ এটা মাত্র নতুন পদার্থ উৎপন্ন কৰে।
- বিযোজন বিক্রিয়া সংযোজন বিক্ৰিয়াৰ বিপৰীত। এটা বিযোজন বিক্রিয়াত এটা পদার্থ বিযোজিত হৈ দুটা বা ততোধিক পদার্থ উৎপন্ন কৰে।
- যিবোৰ বিক্ৰিয়াত বিক্রিয়াজাত পদাৰ্থৰ লগতে তাপ উৎপন্ন হয় সেইবোৰক তাপবর্জী বিক্রিয়া বোলে।
- যিবোৰ বিক্ৰিয়াত তাপ শোষিত হয় সেইবোৰক তাপগ্রাহী বিক্রিয়া বোলে।
- যেতিয়া এটা মৌলই আন এটা মৌলক তাৰ যৌগ এটাৰ পৰা অপসাৰিত কৰে, তেতিয়া এটা অপসৰণ বা প্রতিষ্ঠাপন বিক্রিয়া ঘটে।
- দ্বিঅপসৰণ বিক্ৰিয়াত দুটা বিক্ৰিয়াৰ দুটা বেলেগ বেলেগ পৰমাণু বা পৰমাণুৰ থুপ (আয়ন) ৰ পৰস্পৰৰ লগত স্থান বিনিময় ঘটে।
- অধঃক্ষেপন বিক্রিয়াত অদ্রাব্য লৱণ উৎপন্ন হয়।
- কিছুমান বিক্রিয়াত পদার্থই অক্সিজেন বা হাইড্র'জেন লাভ কৰে বা হেৰুৱায়। জাৰণত পদার্থই অক্সিজেন লাভ কৰে বা হাইড্ৰ'জেন হেৰুৱায়। বিজাৰণত অক্সিজেন হেৰুৱায় আৰু হাইড্র'জেন লাভ কৰে।
♦ ৰাসায়নিক সমীকৰণ (Chemical Equation)
- ৰাসায়নিক বিক্ৰিয়া এটাত অংশ গ্ৰহণ কৰা পদাৰ্থ বোৰ চিহ্ন আৰু সংকেতৰ সহায় ত উপস্থাপন কৰিলে তাক ৰাসায়নিক সমীকৰণ ইয়াক শব্দ ৰূপত প্ৰকাশ কৰিলে তাক শব্দ সমীকৰণ বুলি কোৱা হয় |
উদাহৰণ -
2Mg + O2 ⟶ 2MgO
♦ বিক্ৰিয়ক আৰু বিক্ৰিয়াজাত পদাৰ্থ
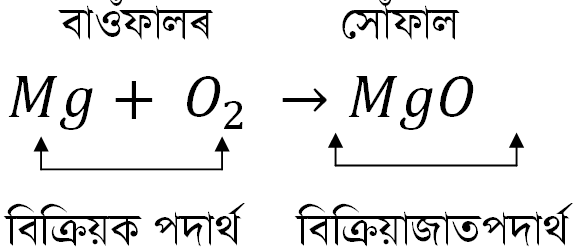
- ৰাসায়নিক সমীকৰণ এটাত কাঁড় চিনৰ বাওঁফালৰ পদাৰ্থ বোৰক বিক্ৰিয়ক পদাৰ্থ বোলে আৰু কাঁড় চিনৰ সোঁফালৰ পদাৰ্থবোৰক বিক্ৰিয়াজাত পদাৰ্থ বোলে |
উদাহৰণ -
♦ সন্তুলিত ৰাসায়নিক সমীকৰণ (Balanced Chemical Equations)
- যি ৰাসায়নিক সমীকৰণত বিক্ৰিয়ক আৰু বিক্ৰিয়াজাত পদাৰ্থৰ প্ৰতিটো মৌলৰ সমান সংখ্যক পৰমাণু থাকে তাকে সন্তুলিত ৰাসায়নিক সমীকৰণ বোলে।
উদাহৰণ -
i. H2 + Cl2 → 2HCl
ii. 2Mg + O2 ⟶ 2MgO
♦ অসন্তুলিত ৰাসায়নিক সমীকৰণ (Balanced Chemical Equations)
- যি ৰাসায়নিক সমীকৰণ এটাত বিক্ৰিয়ক আৰু বিক্ৰিয়াজাত পদাৰ্থৰ মুঠ ভৰ সমান নাথাকিলে তাক অসন্তুলিত ৰাসায়নিক সমীকৰণ বা জঁকা ৰাসায়নিক সমীকৰণ বোলে।
উদাহৰণ -
i. H2 + Cl2 → HCl
ii. Mg + O2 ⟶ MgO
YouTube Channel
| Assam TET Academy | Subscribe Now |
| Assam Job Portal | Subscribe Now |
♦ ৰাসায়নিক বিক্ৰিয়াৰ(Chemical Reaction)
- দুটা বা ততোধিক পদাৰ্থ ৰাসায়নিক ভাবে মিলিত হৈ নাইৱা এটা পদাৰ্থ ভাঙি দুটা বা ততোধিক ভিন্ন ভৌতিক তথা ৰাসায়নিক ধৰ্ম বিশিষ্ট নতুন পদাৰ্থ ৰ সৃষ্টি কৰা প্ৰক্ৰিয়াক ৰাসায়নিক বিক্ৰিয়া বোলে |
♦ ৰাসায়নিক বিক্ৰিয়াৰ বৈশিষ্ট্য়
- ৰাসায়নিক বিক্ৰিয়া এটা ঘটিছে নে নাই তাক জানিবলৈ আমি তলত দিয়া পৰিৱৰ্তনবোৰ লক্ষ্য কৰিম |
i. অৱস্থাৰ পৰিৱৰ্তন
ii. ৰঙৰ পৰিৱৰ্তন
iii. গেছৰ উৎপত্তি
iv. উষ্ণতাৰ পৰিৱৰ্তন
v. অধঃক্ষেপন গঠন
♦ ৰাসায়নিক বিক্ৰিয়াৰ প্ৰকাশ(Types of Chemical Reaction)
1. সংযোজন বিক্ৰিয়া (Combination Reaction)
2. বিযোজন বিক্ৰিয়া (Decomposition Reaction)
3. তাপবৰ্জী বিক্ৰিয়া
4. তাপগ্ৰাসী বিক্ৰিয়া
5. অপসৰণ বা প্ৰতিষ্ঠাপন বিক্ৰিয়া
6. দ্বিঅপসৰণ বিক্ৰিয়া
7. অধঃক্ষেপন বিক্ৰিয়া
8. তাপীয় বিযোজন বিক্ৰিয়া
♦ সংযোজন বিক্ৰিয়া (Combination Reaction)
- যি বিক্ৰিয়াত দুই বা ততোধিক বিক্ৰিয়ক পদাৰ্থ লগ হৈ এটা মাত্ৰ বিক্ৰিয়াজাত পদাৰ্থ উৎপন্ন হয় তাকেই সংযোজন বিক্ৰিয়া বোলে |
উদাহৰণ -
i. C + O2 ⟶ CO2
ii. Mg + O2 ⟶ MgO
♦ বিযোজন বিক্ৰিয়া (Decomposition Reaction)
- যি বিক্ৰিয়াত তাপ, পোহৰ বা বিদ্যুৎ শক্তিৰ উপস্থিতিত এটা মাত্ৰ বিক্ৰিয়ক পদাৰ্থ ভাঙি দুটা বা ততোধিক বিক্ৰিয়াজাত পদাৰ্থ উৎপন্ন কৰে তাকেই বিযোজন বিক্ৰিয়া বোলে |
উদাহৰণ -
![]()
♦ বিয়োজন বিক্ৰিয়াৰ প্ৰকাৰ -
i. তাপীয় বিয়োজন বিক্ৰিয়া
ii. আলোক বিয়োজন বিক্ৰিয়া
iii. বিদ্যুৎ বিশ্লেষণ বিয়োজন বিক্ৰিয়া
♦ তাপীয় বিয়োজন বিক্ৰিয়া
- যি বিয়োজন বিক্ৰিয়া তাপ প্ৰয়োজন কৰি ঘটোৱা হয় তাক তাপীয় বিয়োজন বিক্ৰিয়া বোলে |
উদাহৰণ -
![]()
♦ আলোক বিয়োজন বিক্ৰিয়া
- যি বিয়োজন বিক্ৰিয়াত পোহৰ প্ৰয়োগ কৰি ঘটোৱা হয় তাক আলোক বিয়োজন বিক্ৰিয়া বা আলোক বিশ্লেষণ বোলে |
উদাহৰণ -
![]()
SEBA Class 10 in Assamese Medium
| English | অসমীয়া | গণিত |
| বিজ্ঞান | সমাজ | উচ্চ গণিত |
| E.Grammar | অ. ব্যাকৰণ |
♦ বিদ্যুৎ বিশ্লেষণ বিয়োজন বিক্ৰিয়া
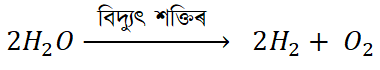
- যি বিয়োজন বিক্ৰিয়া বিদ্যুৎ প্ৰয়োগ কৰি ঘটোৱা হয় তাকে বিদ্যুৎ বিশ্লেষণ বিয়োজন বিক্ৰিয়া বোলে |
উদাহৰণ -
♦ তাপবর্জী বিক্রিয়া
- যিবোৰ বিক্ৰিয়াত বিক্ৰিয়াজাত পদাৰ্থৰ লগত তাপ উৎপন্ন হয় সেইবোৰক তাপবৰ্জী বিক্ৰিয়া বোলে।
উদাহৰণ -
CH4(g) + 2O2(g) → CO2(g) + 2H2O(g)
♦ তাপগ্রাহী বিক্রিয়া
- যি বিক্ৰিয়া সংঘটিত হঁওতে তাপ, পোহৰ নাইবা বিদ্যুৎ শক্তিৰ প্ৰয়োজন হয় অৰ্থ্যাৎ শক্তি শোষণ হয় তেনে বিক্ৰিয়াক তাপগ্ৰাহী বিক্ৰিয়া বোলে।
উদাহৰণ -
![]()
♦ অধঃক্ষেপণ বিক্রিয়া
- যি ৰাসায়নিক বিক্ৰিয়াত অধঃক্ষেপ উৎপন্ন হয় তেনে বিক্ৰিয়াক অধঃক্ষেপ বিক্ৰিয়া বোলে।
উদাহৰণ 一
AgNO3 → AgCl↓ + NaNO3
♦ অপসৰণ বা প্ৰতিষ্ঠাপন বিক্ৰিয়া (Displacement Reaction)
- যি বিক্ৰিয়াত অধিক সক্ৰিয় মৌলই কম সক্ৰিয় মৌল এটাক তাৰ যৌগৰ পৰা অপসাৰিত কৰে |
- অধঃক্ষেপৰ সৃষ্টি নহয় |
অপসৰণ বিক্ৰিয়াৰ সমীকৰণ -
Zn + CuSO4 → ZnSO4 + C
♦ দ্বিঅপসৰণ বিক্ৰিয়া (Double Displacement Reaction)
- যি বিক্ৰিয়াত দুটা বিক্ৰিয়ক পদাৰ্থৰ মাজত আয়নৰ বিনিময় ঘটে |
- অধঃক্ষেপৰ সৃষ্টি হয় |
দ্বিঅপসৰণ বিক্ৰিয়াৰ সমীকৰণ -
AgNO3 + NaCl → AgCl + NaNO3
♦ জাৰণ বিক্ৰিয়া (Oxidation Reaction)
- যি বিক্ৰিয়াত কোনো এটা পদাৰ্থৰ লগত অক্সিজেন যুক্ত হয় তাকে জাৰণ বিক্ৰিয়া বোলে।
উদাহৰণ 一
i. 2Cu + O₂ ⟶ CuO
ii. 2Mg + O₂ ⟶ 2MgO
♦ বিজাৰণ বিক্ৰিয়া (Reduction Reaction)
- যি বিক্ৰিয়াত কোনো এটা পদাৰ্থই অক্সিজেন হেৰুৱায় তেনে বিক্ৰিয়াক বিজাৰণ বিক্ৰিয়া বোলে।
উদাহৰণ -
i. CuO + H2 ⟶ Cu + H2O
ii. ZnO + C ⟶ Zn + CO
| SEBA দশম শ্ৰেণীৰ সাধাৰণ বিজ্ঞানৰ MCQ Paper (Total Questions - 45) | ||
| HSLC বিজ্ঞানৰ MCQ Paper - ২০১৬ | Test | |
| HSLC বিজ্ঞানৰ MCQ Paper - ২০১৭ | Test | |
| HSLC বিজ্ঞানৰ MCQ Paper - ২০১৮ | Test | |
| HSLC বিজ্ঞানৰ MCQ Paper - ২০১৯ | Test | |
| HSLC বিজ্ঞানৰ MCQ Paper - ২০২০ | Test | |
| HSLC বিজ্ঞানৰ MCQ Paper - ২০২১ | Test | |
| HSLC বিজ্ঞানৰ MCQ Paper - ২০২২ | Test | |
| HSLC বিজ্ঞানৰ MCQ Paper - ২০২৩ | Test | |
| HSLC বিজ্ঞানৰ MCQ Paper - ২০২৪ | Test | |
| HSLC বিজ্ঞানৰ MCQ Paper - ২০২৫ | Test | |
♦ জাৰণ-বিজাৰণ বা ৰেডক্স বিক্ৰিয়া (Redox Reaction)
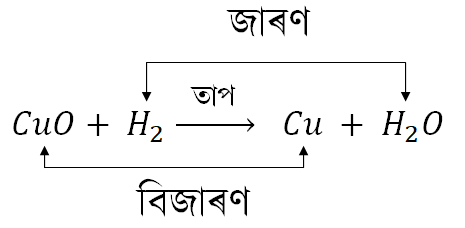
- যিবোৰ বিক্ৰিয়াত এটা বিক্ৰিয়ক পদাৰ্থ জাৰিত হওঁতে আনটো বিজাৰিত হয় তেনেবোৰ বিক্ৰিয়াক জাৰণ-বিজাৰণ বা ৰেডক্স বিক্ৰিয়া বোলে।
উদাহৰণ -
♦ ক্ষয়ীভৱন (Corrosion)
- জলীয় বাষ্প, এছিড আদিৰ প্ৰভাৱত ধাতুৰ পৃষ্ঠভাগৰ অৱক্ষয় সাধন হোৱা প্ৰক্ৰিয়াক ক্ষয়ীভৱন প্ৰক্ৰিয়া বোলে।
উদাহৰণ -
i. ছিলভাৰৰ ওপৰত পৰা কলা চামনি |
ii. ক'পাৰৰ ওপৰত পৰা সেউজীয়া চামনি |
♦ চৰ্বিৰ দুৰ্গন্ধিতা ৰেনচিডিটি (Rancidity)
- তেল অথবা চৰ্বীযুক্ত খাদ্য দীৰ্ঘসময়ৰ কাৰণে ৰাখি দিলে বেয়া গোন্ধ তথা বেয়া স্বাদৰ সৃষ্টি হয় | ইয়াৰ কাৰণ এই যে এনে খাদ্য দ্ৰৱ্যত থকা তেল আৰু চৰ্বী বায়ুৰ অক্সিজেনৰ দ্বাৰা জাৰিত হয় | এই পৰিঘটনাক দুৰ্গন্ধিতা বা ৰেনচিডিটি (Rancidity) বোলে
♦ শব্দ সমীকৰণ
♦ তাপবর্জী বিক্রিয়া আৰু তাপগ্রাহী বিক্রিয়াৰ মাজত পার্থক্য
| তাপবর্জী বিক্রিয়া | তাপগ্রাহী বিক্রিয়া |
| i. এই বিধ ৰাসায়নিক বিক্ৰিয়া, য,ত বিক্ৰিয়াজাত পদাৰ্থ উৎপন্ন হোৱাৰ লগতে তাপ উদ্ভৱ হয় | a. এই বিধ ৰাসায়নিক বিক্ৰিয়া, য,ত বিক্ৰিয়াজা পদাৰ্থ উৎপন্ন হোৱাৰ লগতে তাপৰ শোষণ হয় | |
| ii. সংযোজন বিক্ৰিয়াত তাপ উৎপন্ন হয় | | b. বিযোজন বিক্ৰিয়াত তাপৰ শোষণ হয় | |
| iii. যেনে - C + O2 ⟶ CO2 + তাপ |
c. যেনে - CaCO3 -- তাপ --> CaO + CO2 |
♦ সংযোজন বিক্ৰিয়া আৰু বিযোজন বিক্ৰিয়াৰ মাজত পার্থক্য
| সংযোজন বিক্ৰিয়া | বিযোজন বিক্ৰিয়া |
| i. দুটা বা ততোধিক বিক্ৰিয়ক পদাৰ্থ লগ হৈ এটা মাত্ৰ বিক্ৰিয়াজাত পদাৰ্থ উৎপন্ন হয় | a. এটা বিক্ৰিয়ক পদাৰ্থ দুটা বা ততোধিক বিক্ৰিয়াজাত পদাৰ্থলৈ ভাঙি যায় |
| ii. উদাহৰণ - 2Mg + O2 ⟶ 2MgO |
b. উদাহৰণ - 2H2O ⟶ 2H2 + O2 |
NCERT Class 10 in English Medium
| English | Assamese | Mathematics |
| G.Science | S.Science | Adv. Maths |
| Geography | E.Grammar | অ. ব্যাকৰণ |
| IT(Computer) |
||
♦ জাৰণ বিক্ৰিয়া আৰু বিজাৰণ বিক্ৰিয়াৰ মাজত পার্থক্য
| জাৰণ বিক্ৰিয়া | বিজাৰণ বিক্ৰিয়া |
| i. অক্সিজেন যোগ হয় বা হাইড্ৰ'জেন হেৰুৱায় | | a. অক্সিজেন হেৰুৱায় বা হাইড্ৰ'জেন লাভ কৰে | |
| ii. জাৰক পদাৰ্থই অন্য এটা পদাৰ্থ জাৰিত কৰিব পাৰে | | b. বিজাৰক পদাৰ্থই অন্য এটা পদাৰ্থ বিজাৰিত কৰিব পাৰে | |
| iii. যেনে - 2Cu + O2 ⟶ 2CuO |
c. যেনে - H2 + Cl2 ⟶ 2HCL |
♦ অপসৰণ আৰু দ্বিঅপসৰণ বিক্ৰিয়াৰ মাজত পার্থক্য
| অপসৰণ বিক্ৰিয়া | দ্বিঅপসৰণ বিক্ৰিয়া |
| i. যি বিক্ৰিয়াত অধিক সক্ৰিয় মৌলই কম সক্ৰিয় মৌল এটাক তাৰ যৌগৰ পৰা অপসাৰিত কৰে | | a. যি বিক্ৰিয়াত দুটা বিক্ৰিয়ক পদাৰ্থৰ মাজত আয়নৰ বিনিময় ঘটে | |
| ii. অধঃক্ষেপৰ সৃষ্টি নহয় | | b. অধঃক্ষেপৰ সৃষ্টি হয় | |
| iii. যেনে - Zn + CuSO4 ⟶ ZnSO2 + Cu |
c. যেনে - AgNO3 + NaCl ⟶ AgCl + NaNO3 |
Study Materials (AssamTET.com)
| Assam TET-LP | Assam TET-UP | CTET - Paper 1 |
| CTET - Paper 2 | ADRE Grade 3 | ADRE Grade 4 |
| Assam Police | D.El.Ed | Class 10 |
| Asaam TET-GT | Assam TET-PGT | Class 12 |
Recent Posts
- Assam PNRD Recruitment 2026 – 1508 Vacancies for AE, GRS, Computer Assistant & More | Apply Online
- RRB NTPC Recruitment 2025 – Apply Online for 8850 Graduate & Under Graduate Level Posts
- 2005 voter list download assam
- Assam DElEd Admission 2025 : Online Apply
- Dibrugarh University B.Ed Admission 2025 – DU B.Ed CET Online Form
- SSUHS BPharm & DPharm Admission 2025 – Apply Online
- AIIMS BSc & MSc Nursing Entrance Exam 2025 - Apply Now!
- SSUHS BSc Nursing Admission 2025 – Apply Online
- SAMARTH 2025 : One-Stop Online Portal for Assam College Admissions
- CTET Dec 2018 Paper 2 Question With Answer
- CTET July 2019 Paper 2 Question With Answer
- CTET Dec 2019 Paper 2 Question With Answer
- CTET Dec 2022 Paper 2 Question With Answer
- CTET Aug 2023 Paper 2 Question With Answer
- CTET Jan 2024 Paper 2 Question With Answer
Important Links
- Anundoram Borooah Award 2024 – ARBAS Online Application
- PRC Certificate Assam : How to Online Apply Permanent Residence certificate
- APDCL Recruitment 2024 |Apply Online for 69 Assistant Accounts Officer
- SCERT Assam D.El.Ed Admission 2024 : Online Application Form
- SAMARTH Admission Portal 2024 - Online Apply BA, B.Com and B.Sc Courses
- SSUHS B.Pharm And D.Pharm Admission 2024 – Online Apply
- KKHSOU 2nd Semester UG Courses - Apply Online for 2024 Admission
- KKHSOU 2nd Semester PG Courses - Apply Online for 2024 Admission
- Assam Direct Recruitment Syllabus 2024 – Grade 3 Exam Pattern with pdf
- NEET 2024 Syllabus PDF by NTA




